“Estudio Fase I- II, secuencial durante la fase I, abierto, adaptativo y multicéntrico para evaluar la seguridad, la reactogenicidad y la inmunogenicidad, de un esquema heterólogo de dos dosis del candidato vacunal profiláctico anti SARS – CoV – 2, FINLAY-FR- 2 y una dosis de FINLAY-FR-1A, en niños y adolescentes cubanos”
SOBERANA-PEDIATRÍA
IFV/COR/12
Agosto 2021
SOBERANA02 es una vacuna conjugada, única de su tipo en el mundo para prevenir la COVID-19. Se basa en la conjugación química de la proteína RBD del virus con la proteína toxoide tetánico, una construcción molecular que permite incrementar la inmunogenicidad e inducir memoria inmunológica.
Las vacunas conjugadas surgieron en la historia de la vacunación justamente para inducir protección en niños contra enfermedades infecciosas bacterianas. Existe experiencia de desarrollo de otras vacunas conjugadas en el país que forman parte del esquema ampliado de inmunizaciones que se usa en la población infantil cubana.
El esquema heterólogo de 2 dosis de SOBERANA02 y una dosis de refuerzo con SOBERANA-Plus a intervalos de 28 días, ha demostrado seguridad, inmunogenicidad y eficacia clínica del 91,2% en la prevención de la enfermedad sintomática causada por COVID-19. El 20 de agosto la vacuna SOBERANA02 y SOBERANA-Plus recibieron autorizo de uso en emergencia por la entidad regulatoria nacional, el Centro Estatal para el Control de Medicamentos, Equipos y Dispositivos Médicos (CECMED) para su uso en la prevención de la enfermedad causada por SARS-COV-2 en personas de 19 años o más.
El 10 de junio del 2020, el CECMED aprobó el ensayo clínico “Estudio Fase I/II, aleatorizado, a doble ciego, adaptativo y multicéntrico para evaluar la seguridad, la reactogenicidad y la inmunogenicidad, de los candidatos vacunales profilácticos anti SARS – CoV – 2, FINLAY-FR-1 y FINLAY-FR- 2, en diferentes esquemas, en población pediátrica. El dia 14 de junio comenzó la inclusión y vacunación de los primeros adolescentes de este ensayo clínico. El ensayo se ha desarrollado en el Hospital Pediátrico Juan Manuel Márquez, el policlínico Carlos J. Finlay del municipio Marianao y el policlínico 5 de Septiembre del municipio Playa, en la provincia de La Habana. Los 350 niños incluidos en el ensayo han recibido las dos dosis de SOBERANA02. Todos los niños del subgrupo de 12 a 18 años ya recibieron la dosis de refuerzo con SOBERANA-Plus, así como los de 3-11 de la fase I.
El ensayo tiene como objetivo evaluar la seguridad, la reactogenicidad y la inmunogenicidad del candidato vacunal profiláctico anti SARS-CoV-2, FINLAY-FR- 2 en un esquema heterólogo de dos dosis (0-28) y una tercera dosis con el candidato vacunal FINLAY-FR-1A (día 56) en niños cubanos.
Evidencias de seguridad de la administración de dos dosis SOBERANA02.
El 45% de los sujetos presentó algún evento adverso (42.0% después de la primera dosis y 13.8% después de la segunda dosis). No se reportan eventos adversos graves ni severos. En la evaluación de la seguridad en adultos, se habían reportado eventos adversos en el 45.8% de los sujetos entre 19-29 años y en el 44.2% entre 19-80 años.
El 83,5% de los eventos adversos reportados fueron locales y el 16,5% sistémicos. De tipo local, el evento adverso de mayor frecuencia en los niños de 3 a 18 años fue el dolor (41.1%), con frecuencia similar a los adultos más jóvenes (19-29 años) del estudio fase II (40.1%). Otros eventos de tipo local reportados en los niños y adolescentes fueron aumento de volumen, calor local, eritema e induración (todos con frecuencia inferior al 1%) y solo en el subgrupo etario de 3 a 11 años. Estos eventos también se reportan en los adultos jóvenes y en la población general de la fase II con una frecuencia mayor. De tipo sistémico el evento más frecuente fue el malestar general en 3 adolescentes (0.9%), que también fue el más frecuente en los adultos jóvenes y en la población general, aunque con una frecuencia mayor (1.9% y 3.6%, respectivamente).
La caracterización global de los eventos adversos muestra que el 94,6% de los eventos adversos fue de intensidad leve, solo un 5,4% de intensidad moderada y no se reportaron eventos adversos severos. El 90.2% de los eventos adversos reportados son relacionados con la vacunación. El 100% de los eventos fueron recuperados. El 84.4% de los eventos adversos aparecieron en las primeras 24 horas de administrada la vacuna; el 57.6% de los eventos adversos tuvo una duración de menos de 24 horas; y más del 80% fueron de tipo locales y solicitados.
Estos resultados demuestran que la vacuna SOBERANA02 es segura para su administración en niños y adolescentes; y que el patrón de seguridad global es similar a los adultos.
Resultados de la respuesta inmune en niños vacunados con dos dosis de SOBERANA02.
Las variables inmunológicas de los sujetos de 3-18 años incluidos en la fase I/II, luego de haber recibidos 2 dosis de SOBERANA02, se compararon con los sujetos adultos del ensayo Fase II al mismo tiempo, y con un panel de convalecientes pediátricos conformado a partir de sueros de niños convalecientes que se atienden en el Hospital Juan Manuel Márquez.
Después de dos dosis de SOBERANA02, el 99,3% de los niños de 3-11 años y el 92,9% de los de 12-18 años tuvieron una respuesta de anticuerpos que supera en 4 veces el nivel pre-vacunación (seroconversión) (Figura 1). En el estudio Fase II de adultos el % de seroconversión después de dos dosis fue de 74% en el grupo etario de 19-80 años y de 94,2% para el subgrupo de adultos jóvenes entre 19-29 años. De esta forma, se observa una respuesta superior en los niños entre 3-18 años respecto a los adultos de 19-80 años y similar al subgrupo 19-29 años.
Después de dos dosis de SOBERANA02, la concentración de anticuerpos inducida en los niños de 3-11 años alcanzó una mediana de 99.8 UA/ml (39.1; 216.8) y en los niños entre 12-18 años de 50.3 (15.9; 62.0); comparada con 24 (7.7; 73.0) que se alcanza en los adultos de 19-80 años y con 65.9 (28.4; 189.4) en los adultos entre 19-29 años. El panel de convalecientes pediátricos alcanzó una mediana de 8.7 UA/mL, por lo que la respuesta de anticuerpos inducida por la vacunación con dos dosis de SOBERANA02 es muy superior a la que induce la infección natural en los niños (Figura 1).

Figura 1. Concentración de anticuerpos IgG anti-RBD después de dos dosis de FINLAY-FR2 en niños de 12-18 y 3-11 años comprado con adultos y con panel de niños convalecientes (PNC). UA/mL=anti-RBD IgG concentración expresada en unidades arbitrarias/mL.
El título de neutralización molecular (mVNT50) es una medida de la capacidad de los anticuerpos del suero de inhibir la interacción de la molécula RBD del virus con el receptor ACE2 de la célula humana. En los niños entre 3-11 años se alcanzó un título de neutralización molecular de 327.3 (IC 216.0; 495.9); y en los adolescentes entre 12-18 años es de 161.4 (IC 130.2; 200.0). En adultos del ensayo Fase II, se alcanzaron valores de 106.1 (75.1; 149.9) para los adultos jóvenes y 51,7 (44.4; 60.2) para los adultos en general. El panel de niños convalecientes usado como referencia tiene un título de neutralización molecular de 38.2 (25.6; 57.1). Se puede apreciar que los resultados de la neutralización molecular (mVNT) muestran una mediana y un intervalo de confianza con valores superiores en el subgrupo de los niños entre 3-18 años, respecto a las poblaciones de referencia consideradas. De manera específica, respecto al subgrupo de sujetos entre 19-80 años, los intervalos de confianza para la razón estimada entre la MGT de la neutralización molecular (mVNT50) en cada subgrupo etario respecto a la población de referencia considerada es superior a 1, sugiriendo superioridad, de mayor magnitud en el subgrupo de niños con edades entre 3 y 11 años.
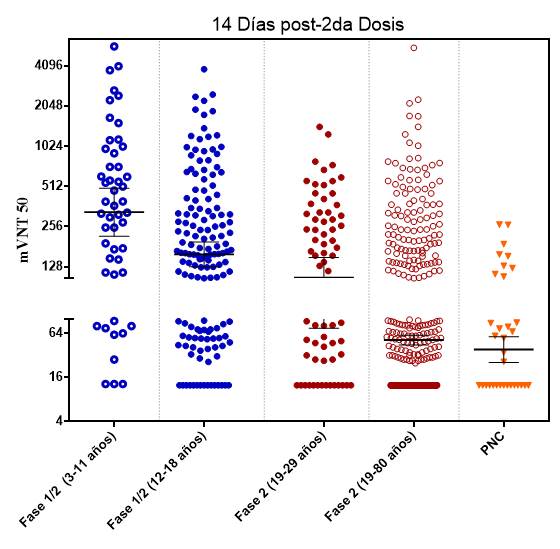
Figura 2. Título de neutralización molecular (mVNT) después de dos dosis de FINLAY-FR2 en niños 12-18 y 3-11 años comprado con adultos y con panel de niños convalecientes (PNC).
Resultados de la respuesta inmune en niños vacunados con dos dosis de SOBERANA02 y una dosis de refuerzo de SOBERANA-Plus.
El efecto de la dosis de refuerzo con SOBERANA-Plus se resume solo para los adolescentes de la Fase I del ensayo (datos disponibles hasta el momento). Con todas las variables inmunológicas se detecta un incremento significativo de los valores posterior a la 3ra dosis. Se logra una seroconversión del 100%, una mediana de concentración de IgG de 358.0 (225.4; 727.2) y una neutralización molecular de 1286.9 (722.2; 2293.4), en todos los casos con diferencias significativas respecto a los niveles alcanzados después de la segunda dosis. La respuesta de anticuerpos después de la tercera dosis muestra un rango similar para la concentración de anticuerpos en los niños de 12-18 años respecto al subgrupo 19-29 años; y superior respecto al grupo de adultos 19-80 y al panel de convalecientes. La neutralización molecular alcanzada después de 3 dosis en los niños 12-18 años muestra una MGT superior respecto al subgrupo de adultos jóvenes, a la población general y al panel de convalecientes pediátricos. (Figura 3).
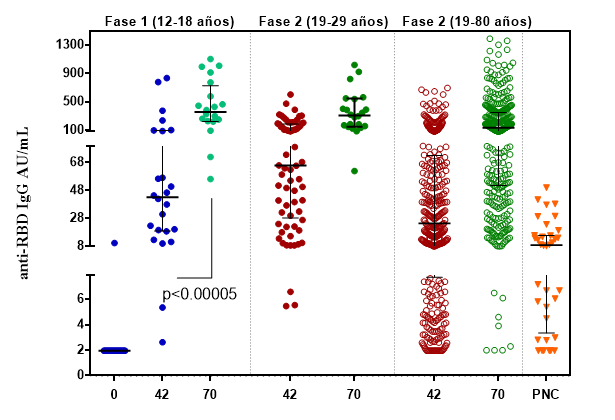
Figura 3. Concentración de anticuerpos IgG anti-RBD después de la 2da y 3ra dosis en niños 12-18 años (Fase I), comparado con adultos y panel de niños convalecientes (PNC).
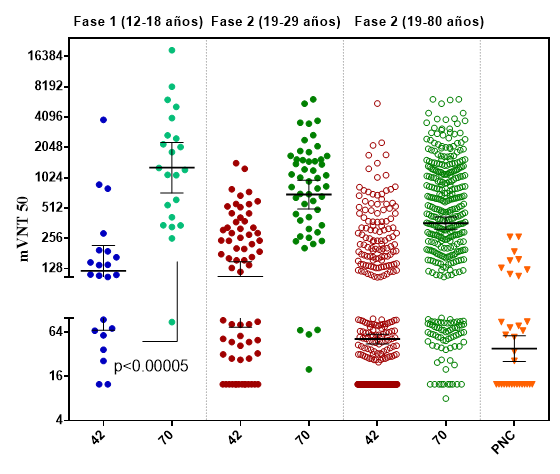
Figura 4. Título de neutralización molecular después de la 2da y 3ra dosis en niños 12-18 años (Fase I), comparado con adultos y panel de niños convalecientes.
Conclusiones del ensayo:
- La vacuna SOBERANA02 es bien tolerada posterior a la administración de dos dosis en niños y adolescentes de 3-18 años de las Fases I/II.
- No se presentaron EA graves ni severos consistentes con la vacunación. La probabilidad de superar la cota de toxicidad prevista es muy baja (Hipótesis de seguridad del estudio).
- El patrón de seguridad es similar al subgrupo de adultos jóvenes (entre 19 y 29 años) del estudio fase II.
- La respuesta inmune (Índice Seroconversión ≥4) es superior al 50% desde los 14 días posteriores a la segunda dosis (Hipótesis de inmunogenicidad) para la Fase I/II de 3-18 años. Se alcanza más de un 90% de seroconversión para la respuesta de anticuerpos específicos anti-RBD después de la segunda dosis para ambos grupos etarios.
- Se observan resultados similares en todas las variables inmunológicas respecto al subgrupo de adultos jóvenes (entre 19 y 29 años) del estudio fase II y superiores al grupo de adultos general (entre 19-80 años).
- Se detecta respuesta inmunológica significativamente superior al panel de convalecientes pediátricos para todas las variables inmunológicas.
- Se detecta un efecto significativo en la respuesta de todas las variables inmunológicas tras la administración de la 3ra dosis en los sujetos entre 12-18 años incluidos en la fase I del ensayo.
Basados en los resultados del ensayo Fase I/II en edades pediátricas con SOBERANA02, el día 27 de agosto se solicita al CECMED una extensión del autorizo de uso de emergencia para población entre 3 y 18 años y se solicita incluir la cohorte de niños entre 2-3 años en el autorizo bajo argumentos clínicos y epidemiológicos avalados por el Grupo Nacional de Pediatría.
El día 3 de septiembre el CECMED autorizó el uso de emergencias para las edades entre 2-18 años. El domingo 5 de septiembre comienza la vacunación de los niños y adolescentes de estas edades, iniciando por la provincia de Cienfuegos y con un cronograma de extensión a todo el país según planificación del MINSAP.



